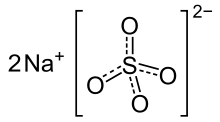
1. Da misure di conducibilità elettrica risulta che la solubilità del solfato di bario BaSO4 in acqua pura è 1.05·10-5 mole/litro a 25°C. Si calcoli il. - ppt scaricare

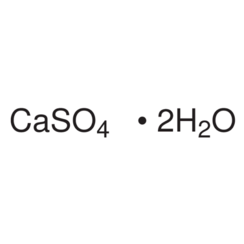
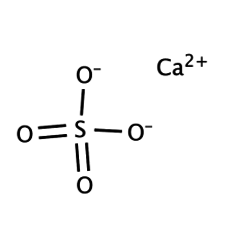
1a) Calcolare la solubilità in g/L del solfato di calcio in acqua deionizzata e in una soluzione di cloruro di calcio 0.50 M. (KPS del solfato di calcio: - ppt video online

LEZIONI DI CHIMICA - Esercizi sul calcolo della concentrazione e della solubilità | Sbobinature di Chimica | Docsity

Esercizi Proposti 3 - esercitazioni sul programma di chimica del primo anno - ESERCIZI PROPOSTI 3: - Studocu

1. Da misure di conducibilità elettrica risulta che la solubilità del solfato di bario BaSO4 in acqua pura è 1.05·10-5 mole/litro a 25°C. Si calcoli il. - ppt scaricare